Технология CRISPR/Cas9 - последние достижения
Обновлено: 29.02.2024
2024. В США одобрили терапию на основе CRISPR для бета-талассемии
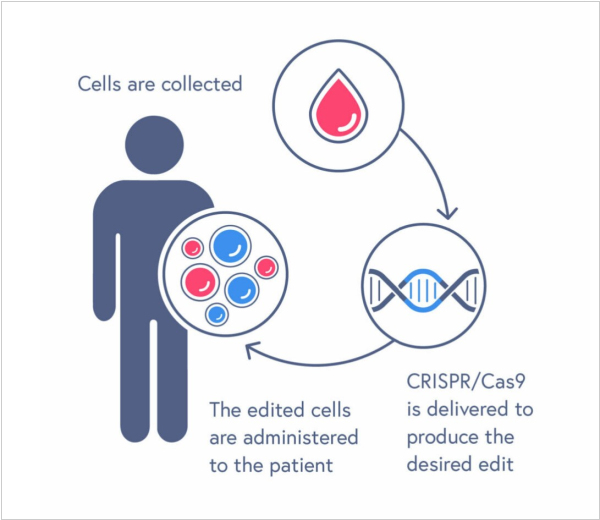
FDA одобрила терапию на основе CRISPR по второму показанию. Им стала бета-талассемия - наследственное генетическое заболевание крови, для которого характерно снижение выработки гемоглобина. Одобрение получил препарат Casgevy компании Vertex Pharmaceuticals. С помощью препарата в кроветворных стволовых клетках, забранных у пациента, выключают ген BCL11A и вводят их обратно в организм. После этого костный мозг начинает вырабатывать фетальный гемоглобин, который замещает собой дефектный. Напомним, впервые CRISPR-терапию одобрили в прошлом году в Великобритании для лечения серповидноклеточной анемии и бета-талассемии.
2023. В Британии одобрили первую в мире CRISPR-терапию для двух заболеваний крови
Управление по контролю лекарственных средств и изделий медицинского назначения в Великобритании разрешило применение первой в мире генной терапии для лечения серповидноклеточной анемии и бета-талассемии для пациентов в возрасте от 12 лет - Casgevy (компании CRISPR Therapeutics). Серповидноклеточная анемии и бета-талассемия - это генетические заболевания, вызванные ошибками в генах гемоглобина. По информации регулятора, Casgevy - первый лицензированный препарат, в котором используется инновационный инструмент редактирования генов CRISPR, за создание которого его изобретатели были удостоены Нобелевской премии в 2020 году. Применение терапии может избавить пациента от необходимости постоянного лечения на долгие годы, потенциально на всю жизнь. В результате тестирования препарата 97% пациентов (28 человек) на год избавились от приступов боли, которая сопровождает заболевание.
2022. Американца вылечили от анемии с помощью CRISPR

Джими Олагер вылечился от тяжелого генетического заболевания — серповидно-клеточной анемии — с помощью генетической терапии на основе CRISPR. У него прекратились приступы боли, и он ни разу не был после терапии в больнице. Серповидноклеточная анемия вызывается мутацией гена гемоглобина, белка, переносящего кислород в крови. Чтобы решить эту проблему, ученые собрали кровь Олагера, использовали CRISPR, чтобы включить производство так называемого фетального гемоглобина, который мы все производим в младенчестве, а затем повторно влили клетки крови обратно в его тело. Компании Crispr Therapeutics и Vertex Pharmaceuticals, которые изготовили тот самый «настой», что вылечил Олагера, планируют представить свою терапию CRISPR в FDA в конце этого года для регистрации. Ранее в этом месяце Crispr и Vertex заявили, что все 31 человек с серповидно-клеточной анемией, получившие лечение, больше не испытывают сильных приступов боли.
2021. Улучшенный CRISPR позволит безопасно исправлять ДНК для лечения муковисцидоза

Муковисцидоз считается одним из наиболее распространенных генетических заболеваний в мире, поэтому, потенциально, технология генного редактирования CRISPR может помочь решить эту проблему. Группа исследователей из Нидерландов использовала редактирование Prime - улучшенную и более безопасную версию CRISPR, который встраивает необходимый фрагмент в ДНК без повреждений где-либо еще. Эксперименты на стволовых клетках человека показали, что лечение исправляет мутации и возвращает клетки к здоровому состоянию. «Мы надеемся, что в будущем это позволит излечивать и предотвращать генетические заболевания у человека. Наша работа — большой шаг к клиническому использованию технологии», — заключил автор работы Маартен Гертс.
2020. Нобелевскую премию по медицине 2020 присудили за открытие вируса гепатита C
Нобелевскую премию по медицине и физиологии 2020 присудили Харви Олтеру, Майклу Хаутону и Чарльзу Райсу за открытие вируса гепатита C. Заболевание, вызванное этим вирусом часто называют «ласковым убийцей» — из-за долгого бессимптомного течения и развязки в виде цирроза и смерти. Еще несколько лет назад хронический гепатит C считался неизлечимым заболеванием. Но с 2013 года появились новые препараты, благодаря которым от вируса безболезненно и почти наверняка можно избавиться за три месяца (хотя стоимость лечения - около $12 тыс за курс). А вот Нобелевскую премию по химии в этом году дали за более новое медицинское достижение - технологию генного редактирования CRISPR/Cas9. Получили ее Эммануэль Шарпантье и Дженифер Дудна.
2020. CRISPR сможет лечить ожирение преобразованием жировых клеток в сжигателей жира

Есть два типа жировой ткани. Коричневая жировая ткань известна как здоровый жир, потому что она сжигает калории, чтобы произвести тепло. Белый жир, напротив, может накапливаться и вызывать ожирение. Группа исследователей из Гарварда под руководством Ю-Хуа Ценг разработала технологию генной модификации клеток белого жира в аналоги клеток коричневого жира (HUMBLE-клетки). Внедрив такие клетки в организм мышки ученым удалось поддерживать ее вес нормальным в условиях очень жирной диеты. Для генной модификации использовалась популярный метод CRISPR.
2019. Verve Therapeutics хочет избавить людей от болезней сердца при помощи CRISPR
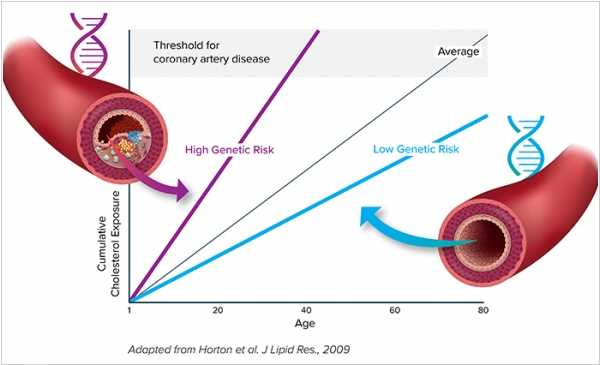
Как известно, одной из основных причин сердечной недостаточности, является наличие в крови «плохого» холестерина, оседающего на стенках сосудов. Причем, у одних людей проблем с этим плохим холестерином - вообще нет, а другим приходится принимать статины, придерживаться диеты и активно заниматься спортом. Причина - в различии определенных генов. Стартап Verve Therapeutics - нашел эти гены и придумал, как их редактировать прямо в организме при помощи CRISPR. Если Verve добьется своего, для снижения риска сердечно-сосудистых заболеваний будет достаточно одной инъекции наночастиц с нужными генами и комплексом CRISPR. В компании не разглашают список участков ДНК, которые предполагается редактировать, однако, скорее всего, это гены, работающие в печени. Verve Therapeutics уже привлек $58,5 млн инвестиций, в том числе от Google.
2019. Фен Жанг теперь умеет редактировать ДНК и РНК с точностью до буквы

Фен Жанг, один из трех ученых, которые изобрели знаменитую технологию редактирования ДНК - CRISPR, не сидит на лавке и не плюет семечки, вспоминая о прошлых заслугах. Недавно он основал собственный стартап Beam Therapeutics и сразу поднял $222 млн инвестиций. Что же так привлекло инвесторов? Оказывается, Жанг уже придумал CRISPR 2.0. Технология называется RESCUE и позволяет с высокой точностью заменять любое азотистое основание - аденин (A), гуанин (G), цитозин (C), тимин (T) - буквы генетического алфавита. По сравнению с первоначальной версией CRISPR - это как резинка и карандаш VS ножницы и клей (стандартный CRISPR может только вырезать целые куски ДНК молекулы и склеивать то, что осталось). Кроме того, RESCUE позволяет редактировать не только ДНК, но и РНК, что намного безопаснее - позволит перепрограммировать клетки лишь на время. В первую очередь Жанг хочет вылечить болезнь Альцгеймера. Говорит, там нужно исправить всего две буквы.
2019. Активация одного гена может вылечить ожирение

Исследователи из Калифорнийского университета в Сан-Франциско (Фумитака Иноуи и Надав Ахитув) нашли ген, ответственный за развитие ожирения. Этот ген регулирует чувство насыщения. Если он не достаточно активен, человек бесконтрольно потребляет пищу, и у него развивается ожирение. Ученые научились активировать этот ген (в мышке) с помощью технологии CRISPRa. От обычной технологии CRISPR эта технология отличается тем, что в геноме не вырезают и не заменяют участки ДНК, а лишь активируют нужный ген. Потом, при желании, его можно опять затормозить, так что технология считается довольно безопасной.
2019. Ученые вылечили смертельную болезнь легких еще до рождения пациента
Недавние эксперименты китайского профессора Хе Цзянькуя по редактированию ДНК человеческих эмбрионов вызвали бурю протестов в научном сообществе. Некоторые страны официально запретили подобные опыты. Но ведь никто не запрещал генетическую модификацию эмбрионов мышек? Этим и воспользовались ученые из Медицинского Университета Пенсильвании под руководством доктора Вильяма Перантеу. Они использовали технологию CRISPR для исправления гена, который вызывает респираторный дистресс-синдром - болезнь легких, которая может привести к смерти ребенка. В отличии от опытов китайского товарища, который редактировал оплодотворенные яйцеклетки, американские господа редактировали уже развитый зародыш в матке. Говорят, что хотя это и более опасно для мамы, но зато более безопасно для зародыша, т.к. редактируются прецизионно только клетки легких.
2018. Технология CRISPR заставила раковые клетки убивать друг друга
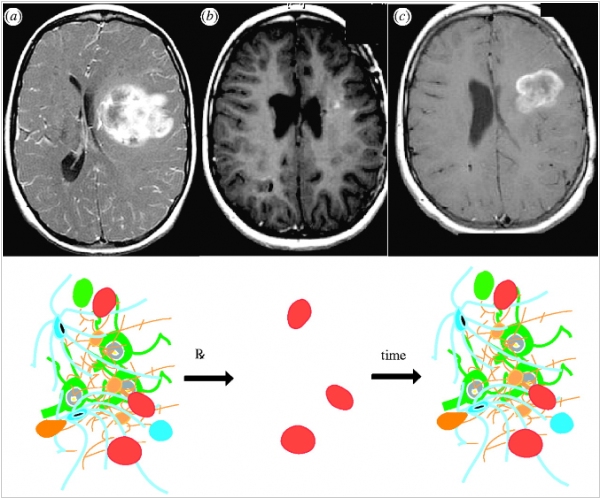
Циркулирующие опухолевые клетки, которые отделяются от первоначального новообразования и вызывают появление метастазов, оказывается, часто возвращаются обратно в опухоль. А значит, их можно использовать для доставки туда препаратов. Ученые из Гарвардской медицинской школы придумали модифицировать такие клетки с помощью технологии CRISPR таким образом, чтобы они вырабатывали белок S-TRAIL, провоцирующий апоптоз - программируемую гибель клетки. Они испытали технологию на мышах с глиобластомой - агрессивной опухолью мозга, и мыши, прошедшие такую терапию, жили дольше.
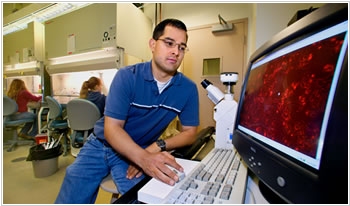
2018. CRISPR-модифицированные клетки печени могут избавить больных гемофилией B от пожизненных инъекций

Пациенты с гемофилией вынуждены в течении всей жизни вводить инъекции с факторами свертывания крови. Команда ученых из Salk Institute (США) под руководством Suvasini Ramaswamy (на фото) хочет избавить их от этой неприятной процедуры. Они провели эксперимент, в ходе которого мышам с гемофилией B ввели генно-модифицированные клетки печени, которые производят фактор свертывания крови и очень обрадовались, т.к. им удалось восстановить свертывание крови на целый год. Подобный метод генотерапии использует стартап Spark Therapeutics, но в отличии от технологии Salk Institute, они редактируют клетки печени прямо в живом организме.
2018. CRISPR-поисковик для диагностики болезней

Технология CRISPR известна, как инструмент для генной терапии, но американский стартап Mammoth Biosciences придумал использовать ее для диагностики заболеваний. Они создали молекулу, которая, находя и вырезая любой заданный фрагмент ДНК или РНК - окрашивается в определенный цвет, так что это можно заметить под микроскопом, изучая биоматериал. Создатели называют свое изобретение ДНК-поисковиком (аля Google), который ищет заданную ДНК-фразу. Технология может выявлять как вирусные инфекции типа малярии, так и онкологические заболевания, типа лейкемии. Одним из сооснователей стартапа является Дженифер Даудна - та самая, которая изобрела технологию CRISPR (блондинка на фото).
2017. CRISPR использовали против болезни Хокинга
Боковой амиотрофический склероз (БАС), которым, в частности, болеет Стивен Хокинг - это медленная, но неизлечимая деградация нейронов, которую связывают с мутациями в определенных генах. Дэвид Шаффер и его коллеги из Калифорнийского университета в Беркли придумали использовать технологию редактирования ДНК CRISPR/Cas9 для замены гена SOD1, который у людей ответственен примерно за 20% случаев БАС. Авторы провели эксперименты на мышах, несших мутантный человеческий ген. Для доставки CRISPR/Cas9 в спинной мозг ученые использовали специальным образом модифицированные аденовирусы, которые практически безопасны для людей. У мышей, прошедших такую экспериментальную терапию, признаки болезни развивались заметно медленнее, и в среднем они жили на месяц дольше – не так мало для положенного этой ГМ-линии 4-месячного срока. Посмертное исследование тканей показало, что в спинном мозге таких животных выжили лишь те двигательные нейроны, в которых произошла успешная замена гена.
2017. CRISPR 2.0 стал точнее в 900 раз
CRISPR-редактирование генов может делать две вещи: исправлять гены и отключать их. Только исправляющая функция работает несколько хуже отключающей. Для исправления вам надо добавить часть ДНК с правильной последовательностью к клеткам и запустить процесс исправления. Это работает только в десятой части клеток, а в клетках мозга не работает вообще. И здесь приходит на помощь открытие Дэвида Лю из Гарвардского университета. Его команда создала инструмент для исправления мутаций, прямо заменяя в ДНК одно азотистое основание на другое. Полученные редакторы оснований ВЕ3 и АВЕ7 меняют основания в половине человеческих клеток, при этом не вызывая практически никаких побочных мутаций.
2017. CRISPR можно использовать для ранней диагностики рака и инфекций

Знаменитая технологии редактирования ДНК CRISPR/Cas9 позволяет находить заданный участок ДНК и вырезать его. А что если использовать эту технологию не для редактирования, а для поиска, и не ДНК, а РНК - подумал один из создателей CRISPR/Cas9 Фен Жанг из института Броуда. И изобрел еще одну технологию с говорящим названием SHERLOCK. Зачем она нужна? Дело в том, что клетки, пораженные вирусом или раковые клетки производят определенные цепочки РНК молекул. Если вы найдете такую молекулу - вы диагностируете заболевание. А Фен Жанг утверждает что белок CRISPR может определить присутствие даже одной-единственной молекулы. И что SHERLOCK (когда появится устройство для анализов) способен выявить, например, вирус Зика в крови или моче пациента всего за несколько часов.
2017. Китайцы повысили точность редактирования человеческих эмбрионов до 50%
Пока в США и Европе ученые договорились не редактировать человеческих эмбрионов (из этических соображений), китайцы делают ощутимый прогресс в этом направлении. В прошлом году они экспериментировали на нежизнеспособных эмбрионах и успешность редактирования была очень низкой - около 2%. Конечно, такой процент не устроил бы никаких родителей. Но в этом году они начали эксперименты на жизнеспособных эмбрионах и точность повысилась аж до 50%. Причем, они уже работают над конкретной задачей - предотвращением генетических болезней. Ученые намеренно дали эмбрионам редкие генетические заболевания, а потом попытались вылечить их с помощью CRISPR.
2017. Суд разрешил патентный спор о правах на CRISPR/Cas9

Технология редактирования ДНК CRISPR/Cas9 считается одним из главных инструментов медицины будущего. Но не менее интересная история происходит за кулисами. Технология была изобретена в 2012 году профессором института Бэркли - Дженифер Даудна совместно с Эммануэль Шарпетье из немецкого института Планка. В 2013 другой исследователь Фен Жанг из института Броуда (связанного с MIT) придумал как использовать эту технологию на живых клетках. Кроме того, он успел быстрее Дженифер получить патент на технологию, хотя подал патент на 8 месяцев позже нее. После этого изобретатели рассорились. Каждый со-основал свой стартап, нацеленный на создание конкретных терапий на базе CRISPR/Cas9: Дженифер - Intellia Therapeutics, Эммануэль - CRISPR Therapeutics, а Фен Жанг - Editas Medicine. ***
2017. Разработаны наночастицы для безопасной доставки CRISPR/Cas9 в клетки
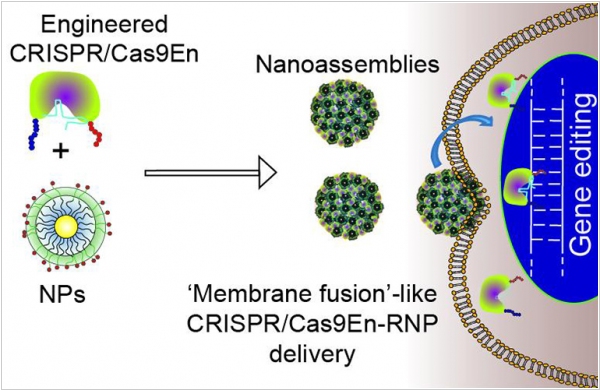
Система редактирования ДНК CRISPR/Cas9 состоит из протеина (который собственно редактирует) и сигнальной РНК (которая помещает его на нужную позицию). Эти штучки работают нормально, но процент успешно-отредактированных клеток все еще остается довольно низким. Причина в том, что доставить протеин и РНК через мембрану клетки в ядро так чтоб они не повредились - довольно сложно. Исследователи из Массачусетского университета Амхерст разработали наночастицы, которые служат в качестве контейнера для CRISPR/Cas9. Они пробивают клеточную мембрану и выпускают груз в цитоплазму клетки. С помощью такой доставки процент успешных редактирований удалось повысить до 30%, что по словам разработчиков - великолепно. Причем, пока они используют технологию только на культивированных в лаборатории клетках, а не в живых организмах.
2016. Китайцы первыми применили технологию CRISPR-Cas9 для лечения человека

Пока американские компании спорят на счет того, кому принадлежать права на революционную технологию редактирования ДНК CRISPR-Cas9 и планируют ее первые клинические испытания, китайцы (из Сычуанского университета) уже умудрились применить эту технологию в реальном кейсе. Они использовали технологию для модификации клеток иммунной системы, взятых у пациента, а затем (когда клетки размножились) ввели их обратно в организм, чтобы те более эффективно боролись с раковыми клетками (рак легких). Напомним, недавно подобную технологию успешно применила и в Великобритании конкурирующая фирма - Cellectis. Но они используют не CRISPR-Cas9, а CAR-T.
2016. Технологию редактирования генома CRISPR/CAS-9 испытают для лечения рака

До сих пор предполагалось, что революционная технология редактирования генома CRISPR/CAS-9 будет впервые испытана на людях в 2017 году (для лечения редкой болезни сетчатки). Однако, вице-президент США Джо Байден (который недавно был назначен главным по борьбе с раком), протолкнул идею более скорого проведения испытания этой технологии для лечения рака (а именно - меланомы, миеломы и саркомы). Финансировать тестирование вызвался тот самый Шон Паркер. Для старта клинических испытаний, которые пройдут в онкологическом центре им. Андерсона (в Техасе), осталось лишь получить разрешение FDA. Во время испытаний у пациентов возьмут имунные Т-клетки, модифицируют их с помощью CRISPR и введут обратно в организм, чтобы они уничтожили опухоль. Напомним, недавно подобную технологию успешно применила в Великобритании конкурирующая фирма - Cellectis.
2016. Новая технология удаляет гены ВИЧ из клеток в живом организме

Исследователи из Темпльского университета (США) под руководством Камела Халили (на фото) впервые успешно вырезали сегмент ДНК, принадлежавший вирусу ВИЧ, из всех клеток в живом организме (мыши) с помощью технологии редактирования генов CRISPR/Cas9. В организмы животных вводили аденовирусный вектор — молекулу, которая содержала в себе необходимые нуклеотидные последовательности, а также гены белка Cas. Через две недели после начала эксперимента оказалось, что сегмент ВИЧ был вырезан из ДНК во всех тканях, в том числе в головном мозге, почках, печени, лёгких, селезёнке и клетках крови. Анализ вирусной РНК показал, что её количество сильно снизилось в клетках лимфоцитов, а также в лимфатических узлах.
2016. Генная терапия останавливает дистрофию мускулов

Сразу три группы американских генетиков заявили о том, что им удалось использовать универсальный генетический редактор CRISPR/Cas9 для того, чтобы вылечить дистрофию мышц (пока у мыши). Дистрофия мышц - это врожденное генетическое заболевание, вызванное повреждением в гене, отвечающей за синтез белка дистрофина. При помощи Фен Чжана (изобретателя CRISPR/Cas9), генетики научились редактировать эти гены. Для доставки препарата был использован модифицированный аденовирус, «боевая часть» которого была заменена на систему CRISPR/Cas и «негативы» заменяемых ей генов. Вирус был введен в кровоток животного. В результате, мускулы начали производить дистрофин и укрепляться, причем это происходило не только в пораженных ногах, но и в сердце и в других частях тела мышей.
2015. Ученые договорились пока не редактировать гены у человеческих эмбионов

В США состоялась крупнейшая конференция, посвященная редактированию генома человека, в которой приняли участие ведущих ученых из Великобритании, США и Китая. И хотя участники единогласно признали перспективность использования генной терапии для лечения генетических заболеваний, они решили пока отказаться от экспериментов по редактированию генов в человеческих эмбрионах. Говорят, это пока слишком опасно. Не только для будущего ребенка (ведь редактирование одних генов может вызвать неизвестные изменения в других), но и для всего человечества (ведь если технология попадет в злые руки - мало ли каких мутантов они могут создать). Напомним, недавно китайский ученый Цзюньцзю Хуан использовал систему редактирования генома CRISPR/Cas9 для удаления опасного гена из ДНК имбрионов, однако метод удачно сработал менее чем в 20 процентах случаев.
2015. Технологию генотерапии CRISPR начнут применять на людях в 2017 году

Катрин Босли, руководитель американской компании Editas (разработавшей знаменитую технологию редактирования ДНК CRISPR-Cas9), заявила, что клинические испытания технологии на людях начнутся в 2017. Для начала компания выбрала редкую болезнь сетчатки Амавроз Лебера, вызывающую врожденную слепоту. Этой болезнью страдают всего лишь 600 человек в США, но именно благодаря этому у Editas будет больше шансов получить сертификацию FDA. Кроме того, сетчатка глаза - одно из наиболее удобных мест для использования генотерапии, т.к. нет проблем с доставкой лекарства (медики умеют делать инъекции прямо в сетчатку). Потенциально же, CRISPR может использоваться для лечения любых генетических болезней. Эта технология позволяет с высокой точностью заменить нужный отрезок ДНК прямо в клетках живого организма.
2015. Видео: как происходит редактирование ДНК методом CRISPR
Открытие технологии CRISPR (в 2013 году) называют лучшим, что случилось в медицине за последние несколько лет. Эта технология позволяет редактировать ДНК отдельных клеток, а теоретически и всех нужных клеток в живом организме. В будущем это позволит целиком удалять из генома взрослого человека дефектные гены - например, вызывающие рак или диабет. Или можно будет отредактировать клетку эмбриона для рождения максимально здорового ребенка нужного пола. Данное захватывающее видео показывает, как именно работает технология CRISPR. Если коротко, CRISPR использует естественную реакцию (иммунитет) клетки на появление чужеродного вируса. Чтобы научиться бороться с вирусом (запомнить его), клетка вырезает часть его ДНК и вставляет в свою ДНК. Таким образом, создавая и запуская в клетку правильный вирус, можно перепрограммировать ее геном.
2013. Американские стартапы разрабатывают технологии генной терапии

Если журнал Science назвал главным прорывом 2013 года в научной медицине иммунотерапию рака, то другой (не менее авторитетный журнал) Nature особо отметил технологию редактирования генома в живых клетках при помощи системы CRISPR, разработанную американским стартапом Editas Medicine. Конечно, генотерапия - круче иммунотерапии, потому что иммунотерапия борется с самим заболеванием, а генотерапия - с его источником - с ошибкой в ДНК. Так вот, новая технология CRISPR якобы позволяет намного дешевле и точнее доставлять редактор ДНК в нужные клетки и надежнее обрезать лишние (вредные) отрезки ДНК, чем существующая технология, использующая вирусы. В первую очередь Editas Medicine планирует использоваться свое генетическое лекарство для лечения нейропсихиатрических расстройств, таких как болезнь Хантингтона и шизофрения. Стартап привлек уже $43 млн инвестиций - а такие деньги на ветер не бросают. ***